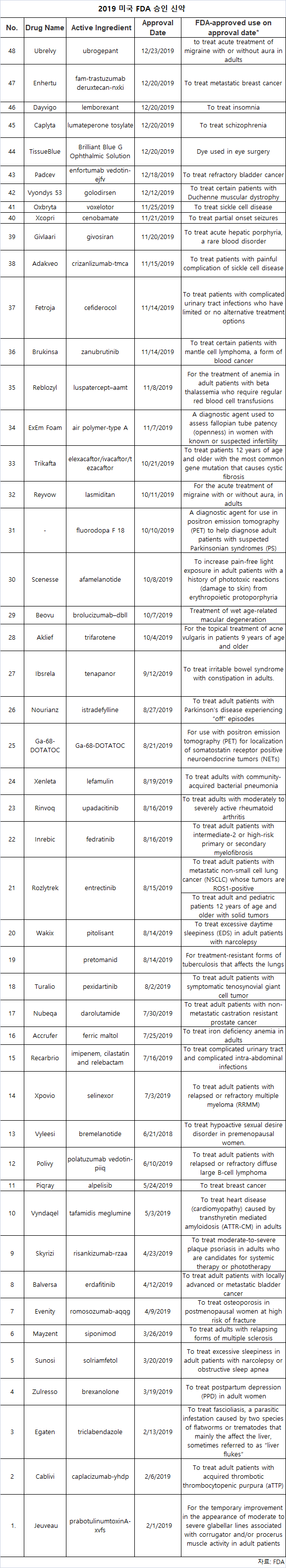
노바티스 6개로 최대 승인…항암제 11개 OK
이는 2018년의 59개 기록에는 미치지 못하지만, 22개만을 승인한 2016년 이후 상승세를 이어가고 있다.
2019년 승인된 새로운 분자 성분(NME) 48개 신약 중 7개(15%)는 12월에, 21개(43%)는 4분기에 청신호를 받았다.노바티스가 2019년 최다 신약을 승인받았다.
회사는 척추근위축증에 대한 유전자 치료제 졸젠스마(Zolgensma) 등 6개 약품에 대해 청신호를 받았다.2018년 4개 항암제로 최다 승인을 받은 화이자와 달리, 노바티스는 유방암 치료제 픽레이(Piqray), 다발 경화증 약품 마이젠트(Mayzent), 겸상 적혈구 치료제 아닥베오(Adakveo), 습성황반변성 약품 비오뷰(Beovu) 등 다양한 질환에 승인을 받았다.
대부분의 경우 다른 업체들은 각각 1개 신약을 허가받았다.로슈, MSD, 다이이찌 산쿄, 애브비 등 일부는 각각 2개 약품에 대해 청신호를 받았다.
이 그룹에서 승자는 740억 달러에 세엘진의 인수로 2년간 신약 고갈에서 벗어난 BMS였다.BMS는 골수섬유증 약품 인레빅(Inrebic), 베타지중해빈혈 치료제 리블로질(Reblozyl) 등 2개 혈액학 자산을 확보했다.
BMS는 2017년과 2018년에 신약 승인없이 톱 15대 제약사에 랭크된 유일한 회사였다.2019년 신약 승인없는 톱 제약사는 GSK, 길리어드, 테바이다.
아스트라제네카는 다이이찌 산쿄와 파트너십으로 유방암 치료제 엔허투(Enhertu)를 허가받지 못했다면 이런 그룹에 포함됐을 것이다.일반적으로 고형암 치료제가 혈액암 약품보다 7대 4로 앞서는 등 항암제는 11개가 승인됐다.
J&J는 방광암에 대한 첫 표적 치료제인 발버사(Balversa)를 승인받았고, 시애틀 제네틱스와 아스텔라스 파마는 전이성 방광암에 대한 항체약품 복합인 파드세브(Padcev)를 조기 승인을 받았다.로슈의 로즐리트렉(Rozlytrek)은 조직 애그노스틱(tissue-agnostic) 약품으로 바이엘과 록소(현 릴리)의 비트락비(Vitrakvi) 시장에 진입했다.
BMS는 희귀암인 골수섬유증의 1차 라인과 후속 치료로 인레빅(Inrebic)을 승인받았다.
로슈의 폴리비(Polivy)와 베이젠의 브루킨사(Brukinsa)는 모두 림프종에 허가됐다.중추신경시스템(CNS) 장애는 7개 신약이 청신호를 받았다.
이 그룹은 AMAG의 성욕감퇴장애 치료제 비리지(Vyleesi), SK 생명과학의 뇌전증 약품 엑스코프리(Xcopri)와 릴리와 엘러간의 각각 편두통 치료제 등이다.세이지 테라퓨틱스의 줄레소(Zulresso)는 산후 장애에 FDA에서 승인된 첫 치료제이고 인트라셀룰라 테라피스의 카플리타(Caplyta)는 정신분열증에 허가됐다.
희귀 의약품과 항생제는 4개가 승인됐다.2가지 종류의 포르피린증(porphyrias)에 알니람의 기블라리(Givlaari)와 클리뉴벨의 사이언시(Scenesse)와 트랜스티레틴 매개 아밀로이드증(ATTR) 치료에 화이자의 빈다퀄(Vyndaqel) 등 3개 희귀약이 승인됐다.
비이익 그룹인 Global Alliance for TB Drug Development은 약물 내성 결핵 약품 프리토마니드(pretomanid)를 승인받았다.일부 약품은 FDA PDUFA 날짜보다 앞서 승인됐다.
버텍스의 낭포성 섬유증 약품 트리캎타(Trikafta), 베이젠의 외투세포림프종 약품 브루킨사(Brukinsa), 노바티스/글로벌 블루드 테라퓨틱스의 겸상적혈구질환 치료제 옥스브리타(Oxbryta), 알니람의 간성 포르피린증 치료제 기블라리(Givlaari), 아스트라제네카/다이이찌 산쿄의 HER+ 유방암 약품 엔허투(Enhertu) 등이 이런 그룹에 속한다.미국 FDA의 신약 수는 매우 일관되게 유지될 것으로 예상된다.
전문가들은 내년에 10~20개의 세포와 유전자 치료제가 FDA에서 승인될 것으로 추정하고 있다.