국내 개발 치료제, 93개 성분·106개 임상 진행중
국내 희귀의약품 시장이 지속적으로 성장하고 있다.
성장세를 이어가기 위해서는 희귀의약품 연구개발 기업들이 국내·외 시장에서 활발한 오픈이노베이션을 통해 성장할 수 있는 정책이 마련돼야 한다는 의견이 나왔다.
한국보건산업진흥원이 최근 ‘국내·외희귀의약품(Orphan Drug) 시장 및 연구개발’ 현황 분석 보고서를 발표했다.
보고서에 따르면 국내·외 희귀의약품 시장은 전체 제약산업의 성장률보다 훨씬 큰 폭으로 성장하고 있으며, 특히 항암 분야와 바이오의약품 및 첨단바이오의약품 연구가 활발히 진행 중이다.
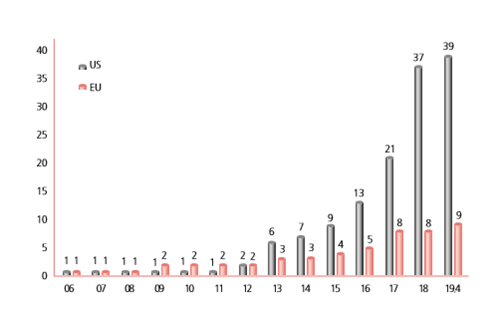
지난해 16개의 의약품, 14개 성분이 미국 FDA 희귀의약품으로 지정 받는 등 2017년 이후 국내 기업의 희귀의약품 지정 건수가 급증했다.
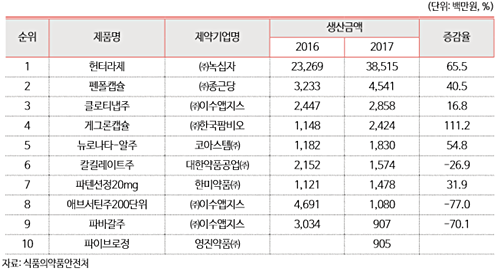
더욱이 녹십자 ‘헌터라제’와 같은 국내 개발 의약품이 수입의약품을 대체하면서 한국 희귀의약품 생산실적이 크게 증가한 것으로 확인됐다.
2017년 희귀의약품 시장규모는 매출액 기준으로 약 1250억불 정도이며, 2024년까지 연평균 11.3% 성장으로 약 2620억불의 시장이 형성될 것으로 예측했다.
이는 처방의약품의 글로벌 시장 성장률 5.3%보다 두 배 이상 높은 수치로, 2024년 전 세계 처방약 매출액의 5분의 1을 차지할 것으로 내다봤다.
또한 미국 FDA의 희귀의약품으로 지정 받은 국내 후보물질은 2015년 2건, 2016년 3건, 2017년 9건, 2018년 16건으로 증가세를 이어가고 있다.
국내 희귀의약품 생산규모는 2013년 216억원에서 2017년 595억원으로 급증했으며, 수입역시 2013년 1247억원에서 2017년 1932억원으로 지속적인 증가 추세를 보이고 있다.
식품의약품안전처, 범부처신약개발사업단, FDA, EMA에 등록된 데이터와 각 기업 홈페이지를 통해 조사한 결과 올해 1월 기준으로 희귀의약품으로 지정을 받았거나, 희귀의약품 지정 대상이 되는 국내 기업 개발 치료제는 93개 성분, 106개의 임상 프로젝트가 진행되고 있는 것으로 확인됐다.
치료 적응증으로 살펴보면 FDA나 유럽에서 희귀의약품으로 지정 받은 총 48개의 건수 중 항암 치료제가 17개로 가장 많았으며 이어서 유전질환 치료제, 감염 치료제 순으로 나타났다.
보고서는 국내 기업의 희귀의약품 개발 전략으로 ▲기존 희귀의약품 치료제의 퍼스트제네릭 ▲신 플랫폼 기술 등을 접목한 개량신약(바이오베터 포함) 개발 ▲적응증에 대한 치료제가 존재하나 새로운 기전에 의한 퍼스트제네릭 개발 ▲치료제가 존재하지 않는 질병에 대한 치료제 개발(First in class) 등 4가지를 제안했다.
먼저 기존 치료제 퍼스트제네릭의 성공적인 사례로 녹십자의 헌터라제를 꼽았으며, 개량신약 개발 전략에는 한미약품의 오락솔(경구용 항암제), 제넥신의 GX-H9(인성장 호르몬), 이수앱지스의 ISU-304(혈우병치료제) 등을 소개했다.
이어 적응증에 대한 치료제가 존재하나 새로운 기전에 의한 퍼스트제네릭 개발 전략에는 신라젠의 펙사벡(항암제), 신풍제약의 피라맥스(말라리아 치료제), 큐리언트의 Q203(다제내성 결핵치료제) 등이 예시로 언급됐다.
마지막으로 치료제가 존재하지 않는 질병에 대한 ‘First in class’ 전략에는 종근당의 CKD-504(헌팅턴증후군 치료제), 케미메디의 KH-NDTC(미분화갑상선암)를 소개했다.
보고서는 “희귀의약품이 기존 수입제품보다 훨씬 낮은 가격으로 건강 보험에 등재돼 환자들의 치료비용을 낮추고, 건강보험 재정 부담도 완화되는 결과를 가져왔다”며 “국내 희귀의약품 연구개발 기업들이 국내외 시장에서 활발한 오픈이노베이션을 통해 성장할 수 있도록 지원하는 정책이 지속적으로 확대돼야 할 것”이라고 강조했다.

