FDA 2017년 13개 품목 허가…셀트리온 암젠 등
올해 제약바이오산업 부분에서 가장 핫 한 이슈로 떠올랐던 바이오시밀러 허가 동향이 내년까지 이어질 것으로 보인다.
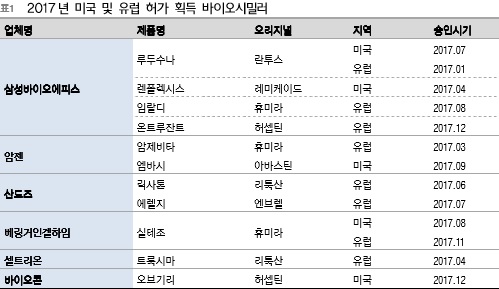
다수의 품목이 임상을 진행 중이거나 허가 대기 중이어서 미국과 유럽을 포함한 다수의 국가에서 바이오시밀러 허가 열풍은 지속될 것으로 예상된다.지난해에는 13종의 바이오시밀러 품목이 FDA와 EMA의 판매 허가를 받았다. 업체별로 살펴보면 삼성바이오에피스 4개, 암젠, 산도즈가 각각 2개, 베링거인겔하임, 셀트리온, 바이오콘 등이 1개 품목의 승인을 획득했다.

암젠의 아바스틴 바이오시밀러 엠바시와 허셉틴 바이오시밀러 ABP980, 바이오콘/밀란의 란투스 바이오시밀러 인스트리델, 산도스의 리툭산 바이오시밀러 릭사톤 등이 내년 미국의 허가 대기 명단에 올랐다.
신재훈 이베스트투자증권 애널리스트는 "미국 레미이드 바이오시밀러 시장에서는 인플렉트라의 본격 적인 마팅과 삼성바이오에피스/MSD의 플렉시스 시장진입이 예상된다"면서 "사보험사의 바이오시밀러 채택률이 높아지면서 시장은 성장할 것"이라고 전망했다.이어 "유럽에서 셀트리온의 트룩시마와 산도즈의 릭 사톤은 공격적으로 시장에 침투할 것"이라고 내다보면서 "유럽 허셉틴 바이오시밀러 시장은 2018년부터 열리기 시작할 것으로 보이며 이미 승인을 받은 삼성바이오에피스의 온트루잔트와 2018년 상반기 에 승인을 받을 것으로 예상되는 셀트리온의 허쥬마, 암젠의 ABP980이 시장에서 치열한 경쟁을 할 것"이라고 전망했다.
문윤희 기자
news@pharmstoday.com

