AZ, ‘파센라’ 승인…GSK·테바와 경쟁 시동
아스트라제네카(AZ)가 미국 FDA에서 심각한 천식에 IL-5 억제제 파센라(Fasenra)를 승인받아 GSK, 테바 등과 복잡한 천식 시장에서 경쟁에 돌입했다.
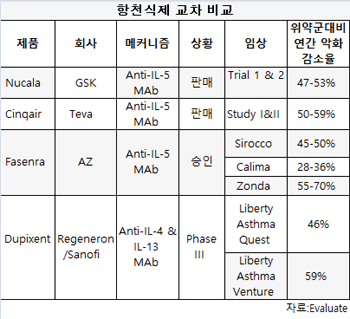
이는 호산성 천식 환자의 치료에 승인이고 호흡기 바이오로직 약품의 AZ의 새로운 포트폴리오에서 첫 번째이다.회사는 IL-5 억제제인 GSK의 뉴카라(Nucala, mepolizumab), 테바의 싱케어(Cinqair/Cinqaero, reslizumab)와 약가로 경쟁을 할 것이라고 밝혔다.
미국에서 파센라는 첫해에 3만 8000달러이지만 유지요법으로 이후 연도에 2만 8000~3만3000달러로 하락할 것으로 예상했다.AZ는 8주에 한번 투여하는 약품의 투여 빈도도 강조하고 있다.
뉴카라와 싱케어는 1개월 용법이다.뉴카라처럼 파센라는 피하주사제인 반면 싱케어는 정맥주입이 필요하다.
파센라는 AZ가 특허만료와 가격 압박으로 타격을 입은 호흡기 프랜차이즈에서 일부 성장의 재추진하기 위해 개발한 3개 호흡기 약품 중 하나이다.
싱케어는 과민증에 대한 블랙박스 경고를 표기하고 있어 파센라의 주요 경쟁자는 뉴카라가 될 것으로 예상된다.또한 사노피/리제너론도 천식 시장에 진입을 준비하고 있다.
회사의 Anti-IL-4/13 억제제인 두피선트(Dupixent)는 현재 FDA 승인을 기다리고 있다.사노피와 파트너인 리제너론의 계획은 호산성 염증과 관련없이 모든 천식 환자에게 두피선트의 승인을 기대하고 있다.
모든 제품은 투여 빈도에서 일부 판가름이 날 것으로 예상된다.파센라는 8주에 한번 투여하는 대신 두피선트는 2주에 한번 뉴카라는 4주에 한번 투여한다.
그러나 효능과 안전성에 대한 우위 없이는 충분한 우위를 점하기 어려울 것으로 예상된다.또한 직접비교와 장기간 데이터가 아직 없어 승리를 단정하기는 어렵다.
선발주자인 뉴카라는 3분기 매출이 9100만 파운드로 전년동기 6000만 파운드에 비해 51.6% 급증했다.
고재구 기자
news@pharmstoday.com

